نشانگرهای زیستی حالت ردوکس تومور در پاسخ به تلفیق مسیرهای آنتی اکسیدانی گلوتاتیون و تیوردوکسین
چکیده
توانایی سلولهای مرکزی سرطان برای حفظ محیط درون سلولی که شدیدا کاهش یافته وابسته به میزان هجوم آن و مقاومت داروها است. سیستم گلوتاتیون و تیوردوکسین برای تنظیم ممانعت ورود ROS ها در فیزیولوژی سلول و برای تحریک اولیه ی تومور و پیشرفت آن، با یکدیگر همکاری می کنند، مسیرهای گلوتاتیون و تیردوکسین به عنوان هدف جدید در سرطان پدیدار شده است. روش های آزمایشگاهی برای تشخیص تغییرات در وضعیت ردوکس تومور در پاسخ به مسیرهای گلوتایتون و تیوردوکسین بوسیله ی مقایسه ی پروب های رزونانس پارامغناطیسی الکترون(EPR) نیتروکساید ردوکس میتوکندریایی و سیتوزولی و تست اعتبارسنجی متقاطع فلوئورسنت دینامیک ردوکس اندازه گیری می شود. بدین منظور، اثر تلفیق کنندگی گلوتاتیون بر بوتیونین سولفوکسیمین(BSO) و مهارکنندگی تیوردوکسین ردوکتاز بر اورانوفین در محیط آزمایشگاه با استفاده از پروب های EPR و roGFP در سلول های سرطان گردن و سینه بررسی شد. در شرایط in vivo موشهایی که دارای زنوگرافت سرطان سینه یا گردن بودند، با تنظیم کننده های گلوتاتیون و تیوردوکسین تیمار شده و با استفاده از پروب چرخش mito-TEMPO بررسی گردیدند. اطلاعات ما به وضوح حاکی از اهمیت استفاده از پروب های چرخشی هدفمند میتوکندریایی برای تشخیص تغییرات در وضعیت ردوکس تومور تحریک شده بوسیله ی تغییردهنده های ردوکس می باشد. بعلاوه باید اعتبار پروب های چرخشی mito- TEMPO درشرایط in vivo از طریق روش های متناوب در شرایط in vivo باید بررسی شود. با این وجود مشخص شده است که پروب چرخشی استفاده شده در شرایط in vivo در زنوگرافت ها، به تغییرات وضعیت ردوکس حساسیت دارند.
مقدمه
سلول های سرطانی میزان تولید گونه های اکسیژن فعال را در مقایسه با سلول های عادی افزایش می دهند(1). گزارشات پیشنهاد می کنند که بوسیله ی سطح میانه ای از ROS، سلول های سرطانی می توانند ROS را در غلظت خاصی که برای پیشرفت تومور ضروری است حفظ کنند(2،3). توانایی سلول های سرطانی مرکزی برای حفظ محیط کاهش یافته ی درون سلولی شدیدا وابسته به مقاومت دارویی و هجوم تومور می باشد(4،5). در بیماران، بیان سطح ژن های آنتی اکسیدان انسانی و نشانگرهای اکسیداتیو وابسته به هجوم تومور و تشخیص ضعیف در بیماران آدنوکارسینومای ریه در مراحل اول است(6). همچنین پارامترهای ردوکس تومور با استفاده از تعیین 62Cu‐ATSM PET در بیماران مبتلا به سرطان گردن و سینه اندازه گیری شد(7). بررسی این مورد اخیرا نشان داد که نسبت اکسیداز برخلاف کاهش گلوتاتیون شدیدا وابسته به کنترل ناحیه ی تومورهای HNSCC است(8). نهایتا اینکه، آنالیز 25 گروه از بیماران مبتلا به سرطان سینه نشان داد که بیان زیاد تیوردوکسین و گلوتاتیون و تیوردوکسین ردوکتاز با کاهش شانس زندگی، افزایش شانس کاهش متاستاز و زندگی بدون بیماری در ارتباط است(9). دیگر مطالعات ارتباط زیادی میان سرطان سلول های ریه (10) و کولورکتال(11) را نشان دادند.
بحث
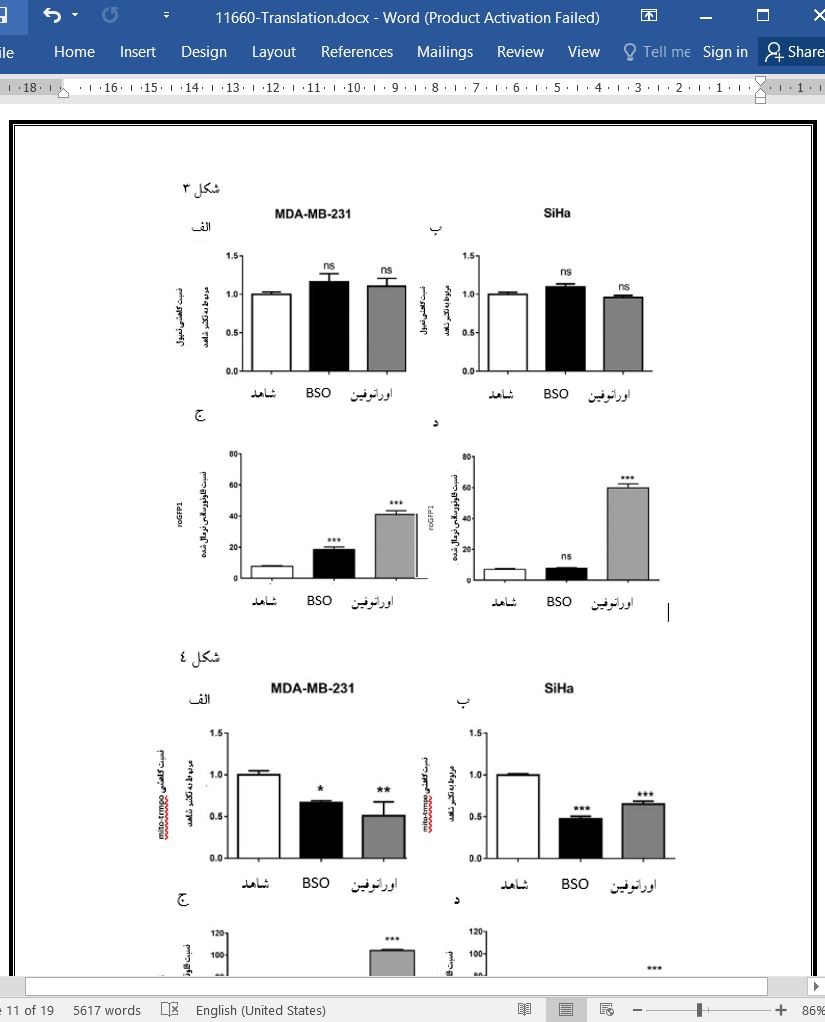
برخلاف سایر تکنیک ها، پروب های چرخشی، توانایی تصویر برداری از وضعیت ردوکس تومور در شرایط in vivo را با استفاده از تصویربرداری EPR یا MRI دارند.(35، 36). اطلاعات ما دو نکته ی مهم در رابطه با تشخیص تغییرات وضعیت ردوکس تومور با استفاده از پروب های چرخشی را نشان می دهد: 1) اهمیت استفاده از پروب های چرخشی با هدف میتوکندریایی برای تشخیص تغییرات در وضعیت ردوکس تومور که در مطالعه ی حاضر در شرایط آزمایشگاه مشخص شد و 2) شناسایی پتانسیل نشان گرهای زیستی ردوکس در پاسخ به تغییرات سیستم گلوتاتیون یا تیوردوکسین در محیط in vivo. با اینکه توانایی داروها برای مقابله با وضعیت ردوکس تومور با استفاده از دوز گلوتاتیون و کیت غیرتخصصی TCA بدست آمد، اطلاعات ما نشان می دهد که پروب چرخشی سیتوزولی tempol برخلاف پروب چرخشی mito-tempo میتوکندریایی، تغییری در وضعیت ردوکس تومور تحریک شده توسط تغییرات مسیرهای گلوتاتیون یا تیوردوکسین در شرایط آزمایشگاه مشخص نکرد. حقیقت این است که کاهش بیشتر سیتوزول نسبت به ماتریکس میتوکندری در سلول های پستانداران ممکن است موجب کاهش حساسیت روش شناسایی در قسمت قبل شود(44،45،46). پروب 1roGFP-mt نیز قادر به نشان دادن تغییرات ایجاد شده توسط BSO یا اورانوفین در هر دولاین سلولی مورد مطالعه بود. این نتایج آزمایشگاهی بدست آمده با نتایج مطالعه ی قبلی که از 2roGFP-1Grx میتوکندریایی و سیتوزولی استفاده شد، در یک راستا هستند، سیتوزول سلول هایی با سنتز معیوب گلوتاتیون، نسبت به تنش اکسیداتیو مقاومت هستند که اکسیداسیون تولید شده در ماتریکس میتوکندری در تیمار BSO معنی دار بود(47).
Abstract
The ability of certain cancer cells to maintain a highly reduced intracellular environment is correlated with aggressiveness and drug resistance. Since the glutathione (GSH) and thioredoxin (TRX) systems cooperate to a tight regulation of ROS in cell physiology, and to a stimulation of tumour initiation and progression, modulation of the GSH and TRX pathways are emerging as new potential targets in cancer. In vivo methods to assess changes in tumour redox status are critically needed to assess the relevance of redox-targeted agents. The current study assesses in vitro and in vivo biomarkers of tumour redox status in response to treatments targeting the GSH and TRX pathways, by comparing cytosolic and mitochondrial redox nitroxide electron paramagnetic resonance (EPR) probes, and cross-validation with redox dynamic fluorescent measurement. For that purpose, the effect of the GSH modulator buthionine sulfoximine (BSO) and of the TRX reductase inhibitor auranofin were measured in vitro using both cytosolic and mitochondrial EPR and roGFP probes in breast and cervical cancer cells. In vivo, mice bearing breast or cervical cancer xenografts were treated with the GSH or TRX modulators and monitored using the mito-TEMPO spin probe. Our data highlight the importance of using mitochondria-targeted spin probes to assess changes in tumour redox status induced by redox modulators. Further in vivo validation of the mito-tempo spin probe with alternative in vivo methods should be considered, yet the spin probe used in vivo in xenografts demonstrated sensitivity to the redox status modulators.
Introduction
Cancer cells sustain a much higher level of ROS production compared to normal cells [1]. Reports have proposed that, by buffering ROS levels, cancer cells can restrict ROS within a range of concentrations that should favor tumor progression [2, 3]. The ability of certain cancer cells to maintain a highly reduced intracellular environment is therefore strongly correlated with aggressiveness and drug resistance [4, 5]. In patients, the expression levels of human antioxidant genes(HAGs) and oxidative markers were related to tumor aggressiveness and predicted poor outcome in patients with early‐stage lung adenocarcinoma [6]. Also, tumor redox parameters measured by 62Cu‐ATSM PET determined the outcome of patients with head and neck cancer [7]. This is in line with a recent study showing that the ratio of oxidized versus reduced GSH was strongly correlated with locoregional control of HNSCC tumors [8]. Finally, analysis of 25 independent cohorts with 5910 breast cancer patients showed that overexpression of thioredoxin (Trx1) and thioredoxin reductase (TrxR1) was associated with a poor overall survival, distant metastasis‐free survival and disease‐free survival [9]. Other studies showed similar correlations in non‐small cell lung carcinoma [10] and colorectal cancer [11].
Discussion
Contrarily to other techniques, spin probes have the potential for in vivo imaging of tumor redox status, using either EPR imaging or MRI [35, 36]. Our data highlight two important findings while assessing the modulation of tumor redox status using spin probes: (i) the importance of using mitochondria‐targeted spin probes to assess changes in tumor redox status, as demonstrated in vitro in the current study, and (ii) the identification of a potential in vivo redox biomarker in response to modulators of the GSH or Trx systems. Despite the ability of the drugs to alter tumor redox status as confirmed using GSH dosage and the non‐ specific ‘TCA’ dosage kit, our data show that the cytosolic spin probe tempol did not detect changes in tumor redox status induced by the modulation of the GSH or Trx pathways in vitro, contrarily to the mitochondrial spin probe mito‐tempo. The fact that the cytosol is maintained more reduced than the mitochondrial matrix in most mammalian cells might reduce the sensitivity of the detection method in the former compartment [44, 45, 46]. The mt‐roGFP1 probe was also able to demonstrate the changesinduced by BSO or auranofin in both cell lines under study. These in vitro results are in line with a previous study, using cytosolic and mitochondrial Grx1‐roGFP2, in which the cytosol of cells with impaired GSH synthesis resisted oxidative stress, while significant oxidation was generated in the mitochondrial matrix upon BSO treatment [47]
چکیده
مقدمه
مواد و روش ها
لاین های سلولی
زنوگرافت در شرایط in vivo
شیمیایی
تیمار دارویی
اندازه گیری EPR در محیط آزمایشگاه
اندازه گیری فلوئورسنت دینامیک ردوکس در محیط آزمایشگاه
آدنوویروس ها
آلودگی با آدنوویروس و درمان
اندازه گیری دینامیک نسبت فلوئورسانس 1- (mt‐)roGFP
اندازه گیری گلوتاتیون درون سلولی
آنالیز ظرفیت آنتی اکسیدانی کل در محیط آزمایشگاه
اندازه گیری EPR در شرایط in vivo
آنالیز آماری
نتایج
ارزیابی مهار هدف
تشخیص تغییرات ردوکس تومور با استفاده از پروب های سیتوزولی در محیط آزمایشگاه
تشخیص تغییرات ردوکس تومور با استفاده از پروب های میتوکندریایی در محیط آزمایشگاه
تشخیص تغییرات ردوکس تومور با استفاده از mito-tempo در شرایط in vivo
بحث
منابع
Abstract
Introduction
Materials and methods
Cell Lines
In vivo xenografts
Chemicals
Drug treatment
In vitro EPR measurements
In vitro redox dynamic fluorescent measurement
Measurement of intracellular GSH
Adenoviruses
Adenoviral infection and treatments
Dynamic measurements of (mt‐)roGFP1 fluorescence ratio
In vitro Total Antioxidant Capacity assay
In vivo EPR measurements
Statistics
Results
Assessment of target inhibition
In vitro assessment of tumor redox changes using cytosolic probes
In vitro assessment of tumor redox changes using mitochondrial probes
In vivo assessment of tumor redox changes using mito‐tempo
Discussion
References
- اصل مقاله انگلیسی با فرمت ورد (word) با قابلیت ویرایش
- ترجمه فارسی مقاله با فرمت ورد (word) با قابلیت ویرایش، بدون آرم سایت ای ترجمه
- ترجمه فارسی مقاله با فرمت pdf، بدون آرم سایت ای ترجمه